Höfundur:
Randy Alexander
Sköpunardag:
2 April. 2021
Uppfærsludagsetning:
1 Júlí 2024

Efni.
Efnajöfna er táknræn framsetning efnahvarfa. Hvarfefni eru skrifuð á vinstri hlið og afurðin á hægri hlið. Lögin um varðveislu massa benda til þess að engin atóm fæðist eða týnist í efnahvörfum, þannig að fjöldi atóma sem eru til staðar í hvarfefninu verður að vera jafn fjöldi atóma sem eru til staðar í hvarfinu. vara. Í kjölfar þessarar kennslu getur þú jafnað efnajöfnur á mismunandi vegu.
Skref
Aðferð 1 af 2: Jafnvægi samkvæmt hefðbundinni aðferð
Skrifaðu uppgefna jöfnu. Í þessu dæmi myndirðu hafa: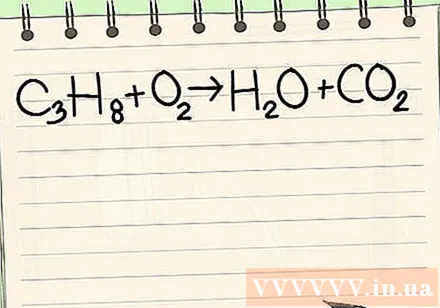
- C3H8 + O2 -> H2O + CO2
- Þessi viðbrögð eiga sér stað þegar própan (C3H8brennt í súrefni til að mynda vatn og koltvísýring.

Skrifaðu niður fjölda atóma fyrir hvert frumefni sem þú hefur á hvorri hlið jöfnunnar. Sjáðu vísitölurnar hér að neðan við hvert atóm til að finna fjölda atóma í jöfnunni.- Vinstri: 3 kolefni, 8 vetni og 2 súrefni.
- Hægri: 1 kolefni, 2 vetni og 3 súrefni.
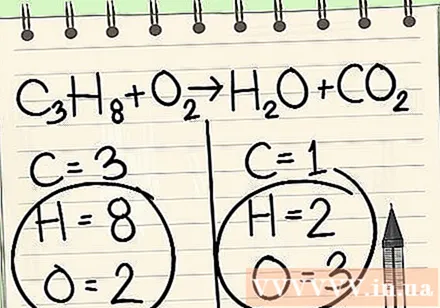
Skildu alltaf vetni og súrefni eftir í lokin.
Ef þú átt fleiri en einn þátt til að halda jafnvægi á: Veldu frumefni sem birtist aðeins í einni sameind hvarfefnisins og aðeins í einni sameind vörunnar. Þetta þýðir að þú verður fyrst að halda jafnvægi á kolefnisatómunum.
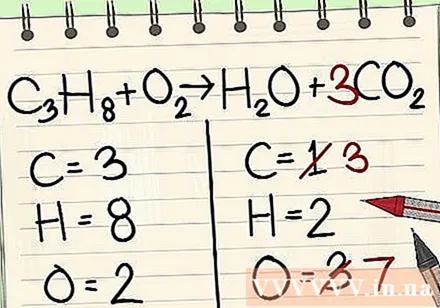
Bætið stuðlinum fyrir einstök kolefnisatóm við hægri hlið jöfnunnar til að koma jafnvægi á hana með kolefnisatómunum þremur vinstra megin við jöfnuna.- C3H8 + O2 -> H2O + 3CO2
- Stuðullinn 3 fyrir framan kolefni hægra megin gefur til kynna að það séu 3 kolefnisatóm þar sem undir-3 til vinstri gefur til kynna 3 kolefnisatóm.
- Í efnajöfnu er hægt að breyta stuðlinum en ekki undirskriftinni.
Næst er atómjafnvægi vetnis. Þú ert með 8 vetnisatóm til vinstri. Þess vegna þarftu 8 hægra megin.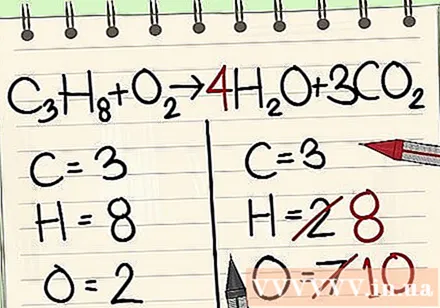
- C3H8 + O2 -> 4H2O + 3CO2
- Til hægri við klukkustundina bætirðu við 4 sem þáttum vegna þess að neðsta talan sýnir að þú ert nú þegar með 2 vetnisatóm.
- Þegar þú margfaldar þátt 4 með vísitölu 2 færðu 8.
- Hin 6 súrefnisatómin eru frá 3CO2. (3x2 = 6 súrefnisatóm + 4 önnur súrefnisatóm = 10)
Jafnvægi súrefnisatóm.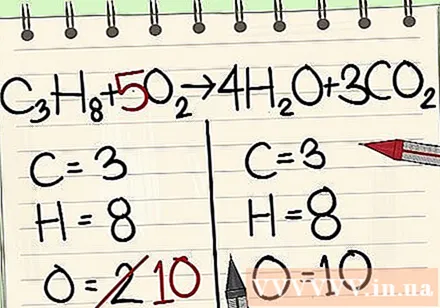
- Vegna þess að þú hefur bætt við stuðlum við sameindirnar til hægri við jöfnuna hefur fjöldi súrefnisatóma breyst. Nú ertu með 4 súrefnisatóm í vatnssameindinni og 6 súrefnisatóm í koltvísýrings sameindinni. Samtals höfum við 10 súrefnisatóm.
- Bættu stuðlinum 5 við súrefnissameindina vinstra megin við jöfnuna. Nú ertu með 10 súrefnissameindir á hvorri hlið.
- C3H8 + 5O2 -> 4H2O + 3CO2.

- Kolefnis-, vetnis- og súrefnisatómin eru í jafnvægi. Jöfnu þín er lokið.
Aðferð 2 af 2: Jafnvægi samkvæmt algebrufræðilegu aðferðinni
Skrifaðu jöfnur eftir táknum og formúlum. Dæmi a = 1 og skrifaðu jöfnuna út frá þeirri formúlu.
Skiptu um tölustafir með breytum þeirra.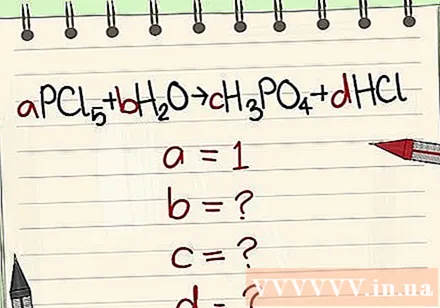
Athugaðu magn þátta í viðbragðshliðinni sem og vöruhliðinni.
- Dæmi: aPCl5 + bH2O = cH3PO4 + dHCl þannig að a = 1 b = c = d = og aðskilja frumefnin P, Cl, H, O, þannig að þú færð a = 1 b = 4 c = 1 d = 5 .
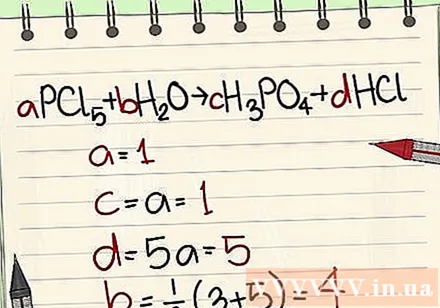
- Dæmi: aPCl5 + bH2O = cH3PO4 + dHCl þannig að a = 1 b = c = d = og aðskilja frumefnin P, Cl, H, O, þannig að þú færð a = 1 b = 4 c = 1 d = 5 .
Ráð
- Mundu að einfalda jöfnuna.
- Ef þú átt í vandræðum geturðu slegið inn jöfnu í jafnvægistækið á netinu til að koma jafnvægi á það. Mundu að þegar þú tekur prófið hefurðu ekki aðgang að jafnvægi á netinu og vertu því ekki háð því.
Viðvörun
- Notaðu aldrei stuðul sem brot í efnajöfnu - þú getur ekki deilt sameindum eða atómum í efnahvörfum.
- Meðan á jafnvægisferlinu stendur er hægt að nota brot en jafnan verður ekki í jafnvægi ef stuðlarnir eru enn brot.
- Til að fjarlægja brot, margföldið alla jöfnuna (bæði til vinstri og hægri) með nefnara brotsins.