Höfundur:
Clyde Lopez
Sköpunardag:
26 Júlí 2021
Uppfærsludagsetning:
1 Júlí 2024
Efni.
- Skref
- Aðferð 1 af 4: Reikna hlutfall með þyngdar- / rúmmálsformúlu
- Aðferð 2 af 4: Undirbúningur sameindalausnar
- Aðferð 3 af 4: Þynningarlausnir þekktrar styrks
- Aðferð 4 af 4: Samræmi við öryggisráðstafanir
- Ábendingar
- Viðvaranir
- Hvað vantar þig
Hægt er að útbúa einfaldar efnafræðilausnir með margvíslegum hætti heima eða í vinnunni. Hvort sem þú ert að búa til lausn úr duftkenndu efni eða þynna vökva, þá er auðvelt að ákvarða rétt magn hvers íhlutar. Við undirbúning efnafræðilegra lausna, mundu að nota persónuhlífar til að forðast skemmdir.
Skref
Aðferð 1 af 4: Reikna hlutfall með þyngdar- / rúmmálsformúlu
 1 Skilgreindu prósentu efni á þyngd/ rúmmál lausnar. Hlutfall sýnir hversu margir hlutar efnis eru í hundrað hlutum lausnar. Þegar það er borið á efnafræðilausnir þýðir þetta að ef styrkurinn er 1 prósent, þá inniheldur 100 millilítrar af lausn 1 gramm af efninu, það er 1 ml / 100 ml.
1 Skilgreindu prósentu efni á þyngd/ rúmmál lausnar. Hlutfall sýnir hversu margir hlutar efnis eru í hundrað hlutum lausnar. Þegar það er borið á efnafræðilausnir þýðir þetta að ef styrkurinn er 1 prósent, þá inniheldur 100 millilítrar af lausn 1 gramm af efninu, það er 1 ml / 100 ml. - Til dæmis, miðað við þyngd: 10% þyngdarlausn inniheldur 10 grömm af efninu sem er leyst upp í 100 ml af lausn.
- Til dæmis, miðað við rúmmál: 23 prósent rúmmál lausn inniheldur 23 millilítra af fljótandi efnasambandi í hverjum 100 millilítra af lausn.
 2 Ákveðið rúmmál lausnarinnar sem þú vilt undirbúa. Til að komast að nauðsynlegum massa efnis verður þú fyrst að ákvarða lokamagn lausnarinnar sem þú þarft. Þetta magn fer eftir því hversu mikla lausn þú þarft, hversu oft þú munt nota hana og stöðugleika fullunninnar lausnar.
2 Ákveðið rúmmál lausnarinnar sem þú vilt undirbúa. Til að komast að nauðsynlegum massa efnis verður þú fyrst að ákvarða lokamagn lausnarinnar sem þú þarft. Þetta magn fer eftir því hversu mikla lausn þú þarft, hversu oft þú munt nota hana og stöðugleika fullunninnar lausnar. - Ef þú þarft að nota ferska lausn í hvert skipti skaltu aðeins útbúa það magn sem þú þarft fyrir eina notkun.
- Ef lausnin heldur eiginleikum sínum í langan tíma geturðu undirbúið stærra magn til að nota hana síðar.
- Dæmi: Þú þarft að búa til 5% NaCl lausn með 500 ml rúmmáli.
 3 Reiknaðu fjölda gramma efnisins sem þarf til að undirbúa lausnina. Til að reikna út nauðsynlegan grömmafjölda, notaðu eftirfarandi formúlu: fjöldi gramma = (hlutfall krafist) (krafist rúmmál / 100 ml). Í þessu tilfelli eru nauðsynlegar prósentur gefnar upp í grömmum og tilskilið rúmmál í millilítrum.
3 Reiknaðu fjölda gramma efnisins sem þarf til að undirbúa lausnina. Til að reikna út nauðsynlegan grömmafjölda, notaðu eftirfarandi formúlu: fjöldi gramma = (hlutfall krafist) (krafist rúmmál / 100 ml). Í þessu tilfelli eru nauðsynlegar prósentur gefnar upp í grömmum og tilskilið rúmmál í millilítrum. - Dæmi: Þú þarft að búa til 5% NaCl lausn með 500 ml rúmmáli.
- fjöldi gramma = (5g) (500ml / 100ml) = 25 grömm.
- Ef NaCl er gefið sem lausn skaltu einfaldlega taka 25 millilítra af NaCl í stað grömm af dufti og draga það rúmmál frá lokamagninu: 25 millilítrum NaCl í 475 millilítra af vatni.
 4 Vegið efnið. Þegar þú hefur reiknað út nauðsynlegan massa efnisins ættir þú að mæla þetta magn. Taktu kvarðaðan kvarða, settu skál á hana og settu núll. Vegið magn af efni er vegið í grömmum og hellt því út.
4 Vegið efnið. Þegar þú hefur reiknað út nauðsynlegan massa efnisins ættir þú að mæla þetta magn. Taktu kvarðaðan kvarða, settu skál á hana og settu núll. Vegið magn af efni er vegið í grömmum og hellt því út. - Áður en haldið er áfram að undirbúa lausnina, vertu viss um að þrífa vigtina af öllum duftleifum.
- Í dæminu hér að ofan þarftu að vega 25 grömm af NaCl.
 5 Leysið efnið upp í nauðsynlegu magni af vökva. Nema annað sé tekið fram er vatn notað sem leysir. Taktu mælagler og mældu nauðsynlega magn vökva. Leysið síðan duftefnið upp í vökvanum.
5 Leysið efnið upp í nauðsynlegu magni af vökva. Nema annað sé tekið fram er vatn notað sem leysir. Taktu mælagler og mældu nauðsynlega magn vökva. Leysið síðan duftefnið upp í vökvanum. - Skrifaðu undir ílátið sem þú munt geyma lausnina í. Gefðu greinilega til kynna efnið og styrk þess á því.
- Dæmi: Leysið 25 grömm af NaCl í 500 ml af vatni til að búa til 5% lausn.
- Mundu að ef þú ert að þynna fljótandi efni, til að fá tilskilið magn af vatni, dragðu rúmmál bætts efnis frá lokamagni lausnarinnar: 500 ml - 25 ml = 475 ml af vatni.
Aðferð 2 af 4: Undirbúningur sameindalausnar
 1 Ákveðið mólþunga efnisins sem notað er með formúlunni. Formúluþyngd (eða einfaldlega mólþungi) efnasambands er skrifuð í grömmum á mól (g / mól) á flöskuvegginn. Ef þú finnur ekki mólþungann á flöskunni skaltu leita á netinu.
1 Ákveðið mólþunga efnisins sem notað er með formúlunni. Formúluþyngd (eða einfaldlega mólþungi) efnasambands er skrifuð í grömmum á mól (g / mól) á flöskuvegginn. Ef þú finnur ekki mólþungann á flöskunni skaltu leita á netinu. - Mólþungi efnis er massi (í grömmum) eins móls af því efni.
- Dæmi: mólþungi natríumklóríðs (NaCl) er 58,44 g / mól.
 2 Ákveðið rúmmál nauðsynlegrar lausnar í lítrum. Það er mjög auðvelt að útbúa einn lítra af lausn, þar sem mólleiki hennar er gefinn upp í mól / lítra, þó getur verið nauðsynlegt að framleiða fleiri eða færri lítra, allt eftir tilgangi lausnarinnar. Notaðu lokamagnið til að reikna út nauðsynlegan fjölda gramma.
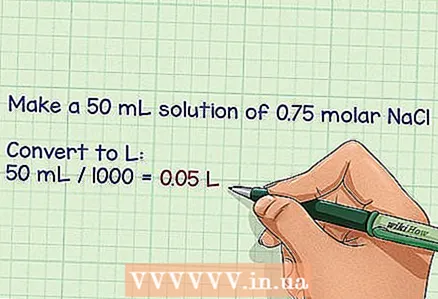
2 Ákveðið rúmmál nauðsynlegrar lausnar í lítrum. Það er mjög auðvelt að útbúa einn lítra af lausn, þar sem mólleiki hennar er gefinn upp í mól / lítra, þó getur verið nauðsynlegt að framleiða fleiri eða færri lítra, allt eftir tilgangi lausnarinnar. Notaðu lokamagnið til að reikna út nauðsynlegan fjölda gramma. - Dæmi: það er nauðsynlegt að útbúa 50 ml af lausn með mólhluta NaCl af 0,75.
- Til að breyta millilítrum í lítra, deildu þeim með 1000 og fáðu 0,05 lítra.
 3 Reiknaðu fjölda gramma sem þarf til að undirbúa nauðsynlega sameinda lausn. Til að gera þetta, notaðu eftirfarandi formúlu: fjöldi gramma = (krafist rúmmáls) (krafist molar) (mólþungi samkvæmt formúlunni). Mundu að nauðsynlegt magn er gefið upp í lítrum, molar í mólum á lítra og mólþungi samkvæmt formúlunni er í grömmum á mól.
3 Reiknaðu fjölda gramma sem þarf til að undirbúa nauðsynlega sameinda lausn. Til að gera þetta, notaðu eftirfarandi formúlu: fjöldi gramma = (krafist rúmmáls) (krafist molar) (mólþungi samkvæmt formúlunni). Mundu að nauðsynlegt magn er gefið upp í lítrum, molar í mólum á lítra og mólþungi samkvæmt formúlunni er í grömmum á mól. - Dæmi: ef þú vilt búa til 50 millilítra af lausn með mólhlutfalli NaCl 0,75 (mólþungi samkvæmt formúlunni: 58,44 g / mól), þá ættir þú að reikna út grömm af NaCl.
- fjöldi gramma = 0,05 l * 0,75 mól / l * 58,44 g / mól = 2,19 grömm af NaCl.
- Með því að minnka mælieiningarnar færðu grömm af efni.
 4 Vegið efnið. Vegið nauðsynlega magn með því að nota rétt kvarðað jafnvægi. Setjið skál á jafnvægið og núllið áður en vegið er. Bætið efninu í skálina þar til þú nærð tilætluðum massa.
4 Vegið efnið. Vegið nauðsynlega magn með því að nota rétt kvarðað jafnvægi. Setjið skál á jafnvægið og núllið áður en vegið er. Bætið efninu í skálina þar til þú nærð tilætluðum massa. - Hreinsið vigtina eftir notkun.
- Dæmi: vegið 2,19 grömm af NaCl.
 5 Leysið duftið upp í nauðsynlegu magni af vökva. Nema annað sé tekið fram nota flestar lausnir vatn. Í þessu tilfelli er tekið sama vökvamagn og var notað til að reikna massa efnisins. Bætið efni í vatn og hrærið þar til það er alveg uppleyst.
5 Leysið duftið upp í nauðsynlegu magni af vökva. Nema annað sé tekið fram nota flestar lausnir vatn. Í þessu tilfelli er tekið sama vökvamagn og var notað til að reikna massa efnisins. Bætið efni í vatn og hrærið þar til það er alveg uppleyst. - Undirritaðu ílátið með lausninni. Merktu uppleyst efni og molatilfinningu greinilega svo að þú getir notað lausnina síðar.
- Dæmi: Notaðu bikarglas (mælimælitæki) til að mæla 50 ml af vatni og leysa upp 2,19 grömm af NaCl í því.
- Hrærið lausninni þar til duftið er alveg uppleyst.
Aðferð 3 af 4: Þynningarlausnir þekktrar styrks
 1 Ákveðið styrk hverrar lausnar. Við þynningu lausna þarftu að þekkja styrk upphaflegu lausnarinnar og lausnina sem þú vilt fá.Þessi aðferð hentar til að þynna einbeittar lausnir.
1 Ákveðið styrk hverrar lausnar. Við þynningu lausna þarftu að þekkja styrk upphaflegu lausnarinnar og lausnina sem þú vilt fá.Þessi aðferð hentar til að þynna einbeittar lausnir. - Dæmi: Undirbúið 75 millilítra af 1,5 M NaCl lausn úr 5 M. lausn. Stofnlausnin hefur styrk 5 M og það er nauðsynlegt að þynna hana í styrk 1,5 M.
 2 Ákveðið rúmmál endanlegrar lausnar. Það er nauðsynlegt að finna rúmmál lausnarinnar sem þú vilt fá. Þú verður að reikna út lausnina sem þarf til að þynna þessa lausn í æskilegan styrk og rúmmál.
2 Ákveðið rúmmál endanlegrar lausnar. Það er nauðsynlegt að finna rúmmál lausnarinnar sem þú vilt fá. Þú verður að reikna út lausnina sem þarf til að þynna þessa lausn í æskilegan styrk og rúmmál. - Dæmi: Undirbúið 75 millilítra af 1,5 M NaCl lausn úr upphaflegri 5 M. lausn. Í þessu dæmi er lokamagn lausnar 75 ml.
 3 Reiknaðu rúmmál lausnarinnar sem þarf til að þynna upphafslausnina. Til að gera þetta þarftu eftirfarandi formúlu: V1C1= V2C2þar sem V.1 - rúmmál nauðsynlegrar lausnar, C1 - styrkur þess, V2 - rúmmál endanlegrar lausnar, C2 - einbeitingu hans.
3 Reiknaðu rúmmál lausnarinnar sem þarf til að þynna upphafslausnina. Til að gera þetta þarftu eftirfarandi formúlu: V1C1= V2C2þar sem V.1 - rúmmál nauðsynlegrar lausnar, C1 - styrkur þess, V2 - rúmmál endanlegrar lausnar, C2 - einbeitingu hans. - Til að reikna út rúmmál nauðsynlegs vökva er nauðsynlegt að endurskrifa jafnréttið með tilliti til V1: V1 = (V2C2) / C1.
- Dæmi: Þú þarft að útbúa 75 ml af NaCl lausn með 1,5 M styrk úr lausn með styrkinni 5 M.
- V1 = (V2C2) / C1 = (0,075 l * 1,5 M) / 5M = 0,0225 l.
- Breytið lítrum aftur í millílítra með því að margfalda með 1000 til að fá 22,5 millilítra.
 4 Dragðu rúmmál upphaflegu lausnarinnar frá fyrirhuguðu lokamagni. Vegna þynningar lausnarinnar er nauðsynlegt að fá fast lokamagn. Dragðu rúmmál lausnarinnar frá lokamagni til að ákvarða rúmmál þynningarlausnarinnar.
4 Dragðu rúmmál upphaflegu lausnarinnar frá fyrirhuguðu lokamagni. Vegna þynningar lausnarinnar er nauðsynlegt að fá fast lokamagn. Dragðu rúmmál lausnarinnar frá lokamagni til að ákvarða rúmmál þynningarlausnarinnar. - Dæmi: Endanlegt rúmmál er 75 millilítrar og upphaflega rúmmálið er 22,5 millilítrar. Þannig fáum við 75 - 22,5 = 52,5 ml. Það er þetta rúmmál vökva sem þarf til að þynna lausnina.
 5 Blandið útreiknuðu magni af lausninni með þynningarvökvanum. Notið bikarglas (tæki til að mæla rúmmál vökva), mælið út nauðsynlegt magn af lausninni og blandið því saman við nauðsynlegt rúmmál þynningarvökvans.
5 Blandið útreiknuðu magni af lausninni með þynningarvökvanum. Notið bikarglas (tæki til að mæla rúmmál vökva), mælið út nauðsynlegt magn af lausninni og blandið því saman við nauðsynlegt rúmmál þynningarvökvans. - Dæmi: Mælið út 22,5 millilítra af 5 M NaCl stofnlausn og þynnið með 52,5 millilítrum af vatni. Hrærið lausninni.
- Skrifaðu á ílátið með þynntu lausninni styrk þess og samsetningu: 1,5 M NaCl.
- Mundu að ef þú ert að þynna sýru með vatni, þá ættir þú að bæta sýru við vatnið, en aldrei öfugt.
Aðferð 4 af 4: Samræmi við öryggisráðstafanir
 1 Notaðu persónuhlífar. Þegar unnið er með árásargjarn efni og lausnir, verndið gegn áhrifum þeirra. Vertu viss um að vera með rannsóknarstofu, lokaða skó, öryggisgleraugu og hanska.
1 Notaðu persónuhlífar. Þegar unnið er með árásargjarn efni og lausnir, verndið gegn áhrifum þeirra. Vertu viss um að vera með rannsóknarstofu, lokaða skó, öryggisgleraugu og hanska. - Notaðu rannsóknarstofuhúð úr óbrennanlegu efni.
- Öryggisgleraugu eiga að vera með hliðarhlífum sem hylja augun frá hliðinni.
 2 Vinna á vel loftræstum stað. Þegar lausnirnar eru blandaðar er hægt að losa rokgjarnar lofttegundir. Sum efni ætti aðeins að meðhöndla undir rannsóknarstofuhettu. Ef þú ert að blanda lausnum heima skaltu opna glugga og kveikja á viftu til að tryggja nægilega loftrás.
2 Vinna á vel loftræstum stað. Þegar lausnirnar eru blandaðar er hægt að losa rokgjarnar lofttegundir. Sum efni ætti aðeins að meðhöndla undir rannsóknarstofuhettu. Ef þú ert að blanda lausnum heima skaltu opna glugga og kveikja á viftu til að tryggja nægilega loftrás.  3 Bætið sýru í vatn. Þegar þykknar sýrur eru þynntar skal ávallt bæta sýrunni út í vatnið. Þegar vatni og sýru er blandað kemur fram exothermic (með losun hita) viðbragða, sem getur leitt til sprengingar ef vatni er bætt í sýruna en ekki öfugt.
3 Bætið sýru í vatn. Þegar þykknar sýrur eru þynntar skal ávallt bæta sýrunni út í vatnið. Þegar vatni og sýru er blandað kemur fram exothermic (með losun hita) viðbragða, sem getur leitt til sprengingar ef vatni er bætt í sýruna en ekki öfugt. - Mundu eftir öryggisráðstöfunum í hvert skipti sem þú vinnur með sýrur.
Ábendingar
- Áður en þú byrjar skaltu kynna þér efnið. Þekking er máttur!
- Prófaðu að nota venjulegar heimilisvörur. Ekki reyna að gera neitt óvenjulegt. Ef þig grunar að hætta geti skapast skaltu gefast upp.
Viðvaranir
- Ekki blanda bleikju og ammoníaki.
- Notaðu öryggisbúnað, hlífðargleraugu, svuntu úr plasti og hanska úr neopreni eftir þörfum.
Hvað vantar þig
- Nákvæmar vélrænni eða rafræn vog til að ákvarða massa. Til dæmis er hægt að nota eldhúsvog.
- Útskrifað glervörur. Þessar áhöld er að finna í eldhúsbúnaðarverslun eða panta á netinu. Mæligler er til í ýmsum stærðum og gerðum. Plastdiskar munu virka, þó þeir þoli ekki hátt hitastig.